Sorprendente somiglianza tra le sincitine umane e la proteina spike sars-cov-2: perché i vaccini covid-19 potrebbero influire sulla fertilità.
L’informazione libera e indipendente ha bisogno del tuo aiuto. Ora più che mai… Database Italia non riceve finanziamenti e si mantiene sulle sue gambe. La continua censura, blocchi delle pubblicità ad intermittenza uniti agli ultimi attacchi informatici non ci permettono di essere completamente autosufficienti.
Fai una donazione seguendo il link sicuro qui sotto
SOSTIENI DATABASE ITALIA
[by Roxana Bruno, Biochemistry PhD in Immunology].
I vaccini COVID-19 trasportano la proteina spike (S o “Spike”) del virus SARS-CoV-2 come presunto antigene per attivare la risposta immunitaria, che condivide un’elevata somiglianza genetica e proteica con due proteine umane, Sincitina-1 e Sincitina -2.
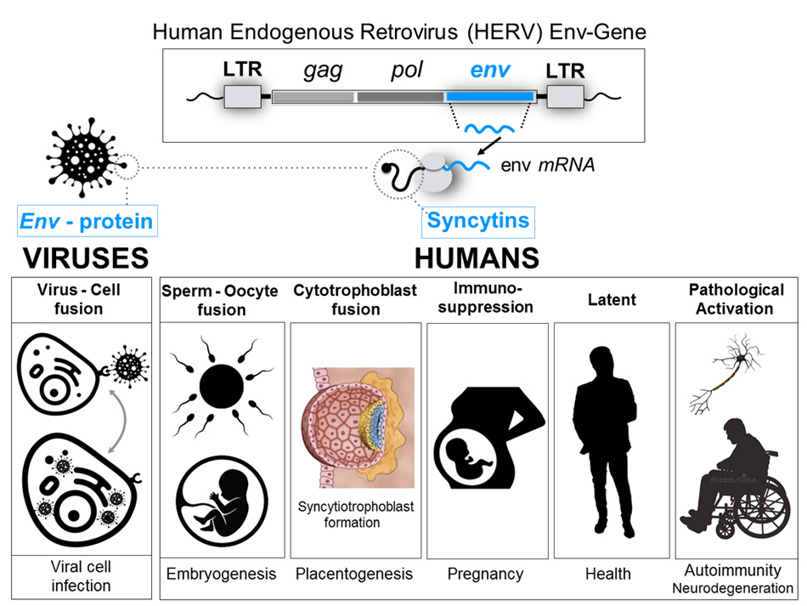
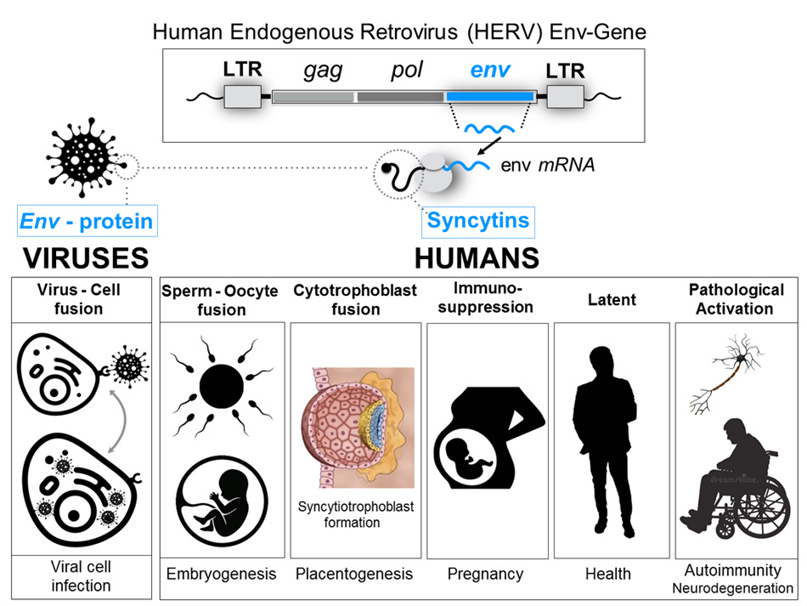
Le sincitine umane sono il prodotto dell’espressione dei geni dell’involucro (Env) dei retrovirus endogeni umani (HERV): sono proteine che mediano la fusione tra le cellule e hanno proprietà immunosoppressive.
Le sincitine sono espresse fisiologicamente durante la gravidanza: intervengono nello sviluppo della placenta, nel differenziamento dei trofoblasti, nell’impianto dell’embrione nell’utero materno e nell’immunosoppressione del sistema immunitario della madre per prevenire il rigetto allogenico dell’embrione.
A causa della somiglianza tra le sincitine e la proteina spike di SARS-CoV-2, le risposte anticorpali indotte dal vaccino COVID-19 potrebbero innescare una reazione crociata contro le sincitine, causando effetti collaterali allergici, citotossici e / o autoimmuni che interessano la salute umana e la riproduzione.
I vaccini a mRNA hanno il potenziale per modificare il DNA umano mediante il meccanismo del silenziamento genico mediato dall’RNA di interferenza. Il gene della sincitina potrebbe essere messo a tacere utilizzando inibitori oligonucleotidici antisenso. Quando l’mRNA o la quantità di proteina sincitina diminuisce, si verificano gravi difetti nella placenta, scarsa differenziazione del trofoblasto umano e disfunzione vascolare placentare, con conseguente perdita della gestazione.
Le aziende che sviluppano i vaccini COVID-19 non agiscono in modo etico e responsabile, perché non effettuano studi di sicurezza nei modelli animali appropriati, non rispettano i tempi necessari per rilevare effetti avversi a medio e lungo termine e, inoltre , non forniscono le informazioni sulla vera composizione del vaccino, che considerano “riservata”.
I volontari non vengono adeguatamente informati di tutti i rischi connessi alla vaccinazione. Avanzando e accorciando le fasi sperimentali, le aziende stanno spostando il rischio dagli animali all’uomo, utilizzando le persone come modelli di prova animale.
Le conseguenze dell’inoculazione di geni estranei con vaccini COVID-19 possono essere catastrofiche per il destino dell’umanità, considerando il ruolo delle proteine dell’involucro HERV (sincitine) nella fisiologia umana e i loro possibili effetti patogeni su vari tipi di tumori e malattie autoimmuni.
La sorprendente somiglianza tra le proteine retrovirali umane endogene e la proteina spike SARS-COV-2.
Qualificati ricercatori scientifici e medici stanno avvertendo la comunità internazionale del pericolo rappresentato dai vaccini contro COVID-19 e chiedono alle autorità di interrompere immediatamente le sperimentazioni cliniche di Fase III sui vaccini contenenti la proteina spike (S o “Spike”) mRNA della SARS -Virus CoV-2 [1, 2].
Uno dei motivi di questa richiesta urgente si basa sul fatto che la proteina S, contro la quale i produttori di vaccini competono per sviluppare un vaccino, condivide un alto grado di similarità genetica e proteica (cioè è altamente omologa nella sequenza dei nucleotidi e aminoacidi) a due proteine umane codificate da geni situati sui cromosomi 7 e 6, i cosiddetti Sincitin-1 e Sincitin-2, rispettivamente. (Figura 1)

La Sincitina-1 è la proteina dell’involucro del retrovirus umano endogeno W (HERV-W), la cui funzione è necessaria durante la gravidanza per permettere lo sviluppo della placenta e la differenziazione del trofoblasto [3], poiché interviene nella fusione delle cellule placentari e consente l’impianto dell’embrione nell’utero materno [4].
La Sincitina-2 è la proteina dell’involucro di un altro membro della famiglia HERV (HERV-FRD) ed è anche altamente espressa nella placenta umana [5]. Sebbene entrambe le sincitine 1 e 2 siano proteine che mediano la fusione cellula-cellula dei citotrofi per consentire la formazione dello strato multinucleato del sinciziotrofoblasto durante lo sviluppo placentare, Sincitin-2 (ma non Sincitin-1) ha proprietà aggiuntive, un’attività immunosoppressiva che rende il feto invisibile al sistema immunitario della madre, prevenendo così il rigetto allogenico, poiché l’embrione è un unico ed essere umano irripetibile, geneticamente diverso dalla madre.
La somiglianza tra la struttura delle sincitine e la proteina S SARS-Cov-2 è davvero sorprendente. La proteina delle sincitine mature (proteina dell’involucro, Env, dei retrovirus umani endogeni, HERV) è costituita da un trizio di eterodimeri di due subunità, S1 e S2, legate da un legame disolfuro labile tra le due catene, che viene scisso da Furine dopo S1 legandosi al recettore [7, 8, 9]. (Figura 2)
La struttura delle sincitine è la stessa descritta per la proteina SARS-CoV-2 S. La subunità S1 dello spike si lega al recettore e quindi la separazione tra i due – il taglio effettuato dall’enzima Furine dalle subunità S1 e S2 – consente al virus di entrare nelle cellule [10].
È interessante notare che il virus SARS-CoV-2 ha anche sequenze identiche alle sincitine che gli conferiscono attività immunosoppressiva [11], con cui il virus riesce a rendersi “invisibile” al sistema immunitario della persona infetta.
Perché i vaccini COVID-19 potrebbero influenzare la fertilità umana?
In primo luogo, i vaccini sperimentali contro COVID-19 potrebbero influenzare la fertilità umana a causa dell’elevata somiglianza tra le sincitine e la proteina spike di SARS-CoV-2 11.
Non sappiamo ancora se gli anticorpi generati dall’azione della vaccinazione COVID-19 possano reagire in modo crociato con le sincitine. Se gli anticorpi contro SARS-COV-2 riconoscessero le sincitine umane, queste proteine sarebbero bloccate e neutralizzate dagli anticorpi, rendendole così incapaci di svolgere la loro funzione di fusione dei citotrofosfati fetali, che svolgono un ruolo chiave sia nel processo di impianto dell’embrione che sviluppo placentare. Il risultato sarebbe un aborto spontaneo dell’embrione nelle donne vaccinate, poiché il processo di differenziazione e nidificazione nell’utero materno è impedito da un’inibizione diretta delle sincitine da parte degli anticorpi indotti dall’immunizzazione artificiale con uno qualsiasi dei vaccini COVID-19 sperimentali.
Infatti, questa affermazione è supportata dall’osservazione che l’espressione della sincitina ricombinante in un’ampia varietà di tipi cellulari induce la formazione di sinciti giganti e la fusione di una linea cellulare trofoblastica umana che esprime sincitina endogena può essere inibita da un antisiero antisintetico . Un anticorpo policlonale di coniglio prodotto contro una miscela di peptici Env-W è stato in grado di inibire la fusione cellulare in vitro mediata dalle sincitine umane [12].
Con la stessa logica, potremmo aspettarci che anche gli anticorpi diretti contro lo spike possano riconoscere e neutralizzare la Sincitina 2 in modo incrociato, e quindi la sua attività immunosoppressiva potrebbe essere influenzata, lasciando l’embrione esposto al riconoscimento del sistema immunitario della madre, che potrebbe portare alla materna rigetto immunitario del feto [13].
È stato dimostrato che le proteine dell’involucro HERV (HERV-Env), da un lato, attivano sia un’immunità innata che adattativa, provocando reazioni infiammatorie, citotossiche e apoptotiche. D’altra parte, hanno la capacità di prevenire l’attivazione della risposta immunitaria, presentando proprietà immunosoppressive e agendo come immunoregolatori [14].
Quando c’è un’elevata somiglianza con i motivi del peptide retrovirale endogeno, il sistema immunitario umano può rilevarlo come un antigene distinto e può innescare una risposta allergica, come quelle che si verificano quando gli apteni (ad esempio la penicillina) si legano alle proteine ospiti [11].
Con la vaccinazione contro COVID-19, possono essere indotte anche risposte anticorpali di tipo IgE e ipersensibilità di tipo ritardato da parte dei linfociti T, come è stato osservato nei topi, che dopo l’esposizione a un vaccino SARS, hanno causato loro una risposta allergica [15, 16].
Pertanto, sappiamo già che a causa della somiglianza della proteina spike del virus SARS-CoV-2 con le due proteine umane, Sincitin 1 e Sincitin 2, è improbabile che si ottenga un vaccino COVID-19 sicuro, senza osservare effetti collaterali allergici, citotossici e / o autoimmuni e senza che questi effetti prima o poi influenzino il delicato meccanismo della riproduzione umana.
In secondo luogo, i vaccini sperimentali contro COVID-19 potrebbero influenzare la fertilità umana perché i livelli di espressione dell’acido ribonucleico messaggero (mRNA) dalle sincitine aumentano progressivamente dall’inizio del concepimento, durante il primo trimestre e fino alla fine della gravidanza [17].
Sia la fusione che la differenziazione delle cellule del trofoblasto sono associate ad un concomitante aumento dell’espressione dell’mRNA del gene sincitina (HERV-W env) e della proteina Sincitina. In termini semplici, se la quantità di proteine o mRNA del gene Syncytin diminuisce, si osservano difetti nella formazione della placenta, scarsa differenziazione dei trofoblasti e disfunzione vascolare nella placenta.
È stato dimostrato che i livelli di proteine e di trascrizione del gene sincitina sono significativamente ridotti nelle placente delle donne con ipertensione indotta dalla gravidanza, inclusi i pazienti con preeclampsia e ipertensione gestazionale [18].
Clinicamente, una diminuita espressione e una localizzazione anormale di Sincitin-1 e Sincitina-2 è stata riscontrata nella pre-eclampsia, un disturbo della gravidanza caratterizzato da difetti nella formazione della placenta, scarsa differenziazione dei trofoblasti e disfunzione vascolare nella placenta. Ciò significa che l’espressione alterata del gene sincitina e la posizione cellulare alterata del suo prodotto proteico possono contribuire all’eziologia della pre-eclampsia [19]. In altre parole, la ridotta espressione placentare di sincitina può contribuire a processi di fusione cellulare alterati durante la placentagenesi e la funzione placentare alterata nei disturbi ipertensivi della gravidanza [20].
D’altra parte, la determinazione della Sincitina-1 nello sperma umano e del suo recettore ASCT-2 nell’ovocita umano suggerisce molto probabilmente un ruolo della Sincitina-1 nella fusione di sperma e ovocita durante la fecondazione [21]. Il recettore ASCT-2, ma non Sincitina-1, è espresso in ovociti e il livello di mRNA aumenta con l’aumentare della maturità degli ovociti. Tuttavia, il modo in cui la fusione dei gameti viene eseguita dalle sincitine e dai loro recettori non è ancora chiaro.
Vaccini COVID-19: un esperimento di transgenesi umana su larga scala.
I vaccini mRNA contro il COVID-19 delle società Moderna, Pfizer/BioNtech e CureVac contengono RNA messaggero della proteina spike, che viene somministrato rivestito con nanoparticelle lipidiche di polietilenglicole al fine di eludere i meccanismi del corpo e consentire loro di entrare nelle cellule.
Questa piattaforma di terapia a RNA modificato è totalmente nuova, è una forma sperimentale di inoculazione di geni estranei nel corpo umano che non può essere definita “vaccinazione” poiché non prevede la somministrazione di patogeni attenuati o inattivati come semplici antigeni che stimolano l’immunità. È l’inoculazione nel corpo umano di varianti di geni sintetici iniettabili, in modo che possano penetrare nelle cellule umane e far sì che producano la proteina spike (S) del virus. Si tratta di un vero esperimento di transgenesi, mai eseguito prima nella storia dell’umanità per conferire immunità contro malattie infettive-contagiose trasmesse dall’uomo.
Le aziende di biotecnologia stanno lottando per replicare il fatto che i vaccini a mRNA non hanno la capacità di entrare nel nucleo per modificare il DNA. Spiegano che l’mRNA nel vaccino codificherà solo la glicoproteina spike (S) e la trascriverà semplicemente nel citoplasma cellulare. È interessante notare che esperti e consulenti di organizzazioni sanitarie nazionali e internazionali si astengono dal menzionare il meccanismo di regolazione epigenetica dell’mRNA. La capacità di regolare direttamente l’espressione genica è un meccanismo ampiamente riconosciuto dalla biologia molecolare: il silenziamento genico mediato dagli acidi ribonucleici, il cosiddetto RNA inibitorio (iRNA) [22].
L’Assemblea Nobel del Karolinska Institutet di Stoccolma, Svezia, ha assegnato il Premio Nobel 2006 per la Fisiologia o la Medicina congiuntamente ai ricercatori Andrew Fire (Stanford University School of Medicine, Stanford, California, USA) e Craig Mello (University of Massachusetts Medical School, Worchester , Massachusetts, USA) per la loro scoperta dell’interferenza dell’RNA. Questi scienziati hanno dimostrato il silenziamento genico attraverso l’uso di iRNA [23] a doppio filamento.
Attraverso il meccanismo del silenziamento genico mediato dall’iRNA, i vaccini a mRNA hanno la capacità potenziale di modificare il DNA umano inducendo o silenziando diversi geni nel nostro genoma. L’RNA di interferenza è un meccanismo fondamentale per controllare il flusso di informazioni genetiche nelle cellule.
Nel caso specifico delle sincitine, l’uso di inibitori dell’RNA (siRNA e shRNA), cioè l’uso di oligonucleotidi antisenso specifici del gene della sincitina, ha già dimostrato che il gene può essere silenziato e che l’inibizione dell’espressione dell’Env-W la proteina porta ad una riduzione della fusione e della differenziazione del trofoblasto umano [3].
Attraverso esperimenti in vivo su animali, sono stati effettuati test sulla perdita di funzionalità nell’utero di pecore mediante iniezione di oligonucleotidi antisenso il giorno 8 della gravidanza. Le iniezioni di questi oligonucleotidi hanno bloccato la produzione di proteine dall’involucro del gene ERV nel trofoectoderma delle pecore.
Il trattamento genico specifico per silenziare l’espressione del gene dell’involucro ERV nelle pecore ha inibito la differenziazione delle cellule trofoblastiche binucleate giganti e ha portato alla perdita della gestazione il 20esimo giorno in tutte le pecore che ricevevano oligonucleotidi antisenso [24].
Va notato che i retrovirus endogeni (ERV) sono abbondanti nei genomi dei vertebrati e svolgono un ruolo fondamentale nella riproduzione dei mammiferi, in particolare nella morfogenesi e nell’impianto placentare, motivo per cui ci si potrebbe aspettare un risultato simile dall’inibizione genica specifica delle sincitine 1 e 2 negli esseri umani e nei primati [25] e possibilmente dei due geni env correlati, sincitina A e sincitina B, nei topi [26].
Gli oligonucleotidi antisenso sono progettati per modulare il trasferimento di informazioni dal gene alla proteina, interferendo con la funzione dell’mRNA o pre-RNA. Per ottenere una modulazione efficace dell’espressione genica da parte degli oligonucleotidi antisenso, vengono utilizzate modifiche degli oligonucleotidi che non promuovono la degradazione della RNasi-H dell’RNA bersaglio. Ad esempio, sono progettati per inibire specificamente l’espressione dell’mRNA del gene dell’involucro HERV, in modo che inibiscano lo splicing e / o la traduzione dell’mRNA mediante un meccanismo di blocco sterico, che è indipendente dalla RNasi-H. Oltre agli effetti di questi oligonucleotidi inibitori a breve termine, la regolazione genica a lungo termine può essere ottenuta mediante RNA antisenso espresso intracellulare somministrato da vettori virali [27].
Conoscendo l’elevata omologia che esiste tra la sincitina e la proteina spike del virus SARS-CoV-2 e sapendo che le sequenze oligonucleotidiche che silenziano il gene umano della sincitina hanno un’omologia del 100% con le sequenze del gene spike introdotto nei vaccini, no si può garantire che le iniezioni di mRNA contenute nei vaccini non finiranno per influenzare l’espressione dei geni umani endogeni Syncytin-1 e Syncytin-2.
Questi aspetti di sicurezza e gli effetti avversi dei vaccini VID-19 sulla fertilità umana non vengono valutati nelle sperimentazioni precliniche sugli animali, né nelle sperimentazioni cliniche di fase I, II e III già condotte con volontari non adeguatamente informati di tutti i rischi connessi alla vaccinazione [28].
È importante notare che ci sono autori che sottolineano che i geni della sincitina sono presenti negli esseri umani e nei primati del Vecchio Mondo e differiscono dai geni Env che sono presenti nei roditori [17, 25]. A questo proposito, studi pre-clinici di uno degli mRNA i vaccini candidati sono stati condotti solo su topi e criceti e sono stati pubblicati online alla fine di ottobre 2020 senza revisione tra pari [29] dopo aver avviato studi clinici di fase I e II con volontari.
Inoltre, le clausole di riservatezza che sono state concesse dai governi alle aziende che sviluppano questi vaccini non ci consentiranno di sapere se i costrutti che compongono i vaccini vettorizzati codificano un gene spike SARS-CoV-2 e / o un singolo o doppio iRNA a filamento con resistenza alle nucleasi. Pertanto, non possiamo nemmeno sapere con certezza se i vaccini che introducono RNA modificati abbiano funzione iRNA e se possano mirare a siti specifici lungo la trascrizione dell’RNA di un gene, in questo caso, le sincitine umane, a causa dell’elevata somiglianza che condividono nella sequenza.
Per tutti questi motivi, il risultato dell’inoculazione di questi vaccini sperimentali può finire per portare alla produzione di anticorpi “con efficacia del 95%” ma non si può escludere che, come effetto collaterale, possano bloccare la traduzione di un messaggero RNA che codifica per una normale proteina umana. Sappiamo in anticipo che gli oligonucleotidi antisenso resistenti alla RNasi H forniscono una resistenza completa alle nucleasi, mostrano una buona capacità di targeting, alta efficienza nella cellula e hanno specificità di sequenza [30].
Con gli strumenti di biologia molecolare disponibili oggi, le aziende di biotecnologia possono introdurre modifiche destabilizzanti agli mRNA, possono migliorare l’efficacia degli RNA inibitori e possono quindi attivare un meccanismo alternativo attraverso il quale il filamento rilevato viene rimosso, conferendo all’iRNA una potente attività di silenziamento. Se questi RNA modificati vengono somministrati con i vaccini VID-19, la popolazione mondiale sarà sottoposta a un nuovo e trascurato metodo di terapia genica sperimentale su larga scala, finalizzato a destabilizzare l’espressione dei geni umani iniettando sequenze estranee, con possibile resistenza alle nucleasi e una comprovata capacità di esercitare un controllo epigenico.
Le aziende che sviluppano questi vaccini non stanno agendo in modo etico o responsabile, perché non stanno conducendo studi di sicurezza nei modelli animali appropriati, né rispettano i tempi necessari per osservare gravi effetti avversi a medio e lungo termine, né stanno fornendo il necessario informazioni che considerano “riservate”. Evitando e improvvisando le fasi di sperimentazione preclinica e passando direttamente alle fasi di sperimentazione clinica I, II e III, le aziende stanno spostando il rischio dagli animali all’uomo, utilizzando le persone come modelli di sfida animale.
Insomma, siamo costretti a denunciare che se i governi vogliono attuare una vaccinazione sperimentale massiccia e obbligatoria della popolazione con vaccini che non hanno compiuto le fasi sperimentali e che sono approvati con protocolli di “emergenza”, sono complici di possibili reati contro umanità, perché queste “ nuove ” piattaforme terapeutiche hanno i meccanismi più ampiamente accettati di silenziamento genico indotto dall’RNA inibitore implicitamente e invisibilmente nei loro progetti, i cui effetti sono ben noti alla comunità scientifica internazionale e tuttavia vengono ridotti al minimo dalle aziende farmaceutiche, quando dovrebbero essere valutati prima che questi vaccini siano autorizzati in commercio.
Le conseguenze dell’inoculazione di questi geni estranei nella popolazione con i vaccini VID-19 potrebbero essere catastrofiche per il destino dell’umanità, se consideriamo il ruolo delle proteine dell’involucro HERV (sincitine) nella fisiologia umana e i loro possibili effetti patogeni su diversi tipi di cancro e malattie autoimmuni come la sclerosi multipla [31, 32], la sclerosi laterale amiotrofica [33, 34, 35] e il diabete di tipo 1 [36].
Articolo originale: Why COVID-19 vaccines might affect fertility
Traduzione italiana di Davide Suraci.
Bibliografia
1- Wodarg W. https://www.wodarg.com/impfen/
2- Wodarg W and Yeadon M. Petition to European Medicines Agency Committee for human medicinal products (CHMP) COVID-19 EMA pandemic Task Force (COVID-ETF) Domenico Scarlattilaan 61083 HS Amsterdam The Netherlands. December 1, 2020. https://2020news.de/wp-content/uploads/2020/12/Wodarg_Yeadon_EMA_Petition_Pfizer_Trial_FINAL_01DEC2020_EN_unsigned_with_Exhibits.pdf
3- Frendo JL, Olivier D, Cheynet V, Blond JL, Bouton O, Vidaud M, Rabreau M, Evain-Brion D, Mallet F. Direct involvement of HERV-W Env glycoprotein in human trophoblast cell fusion and differentiation. Mol Cell Biol 2003; 23:3566–3574. PMID: 12724415 PMCID: PMC164757 DOI: 10.1128/mcb.23.10.3566-3574.2003 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC164757/pdf/1493.pdf
4- Mi, S., Lee, X., Li, Xp. et al. Syncytin is a captive retroviral envelope protein involved in human placental morphogenesis . Nature 403, 785–789 (2000). PMID: 10693809 DOI: 10.1038/35001608. https://www.nature.com/articles/35001608
5- Blaise S, de Parseval N, Bénit L, Heidmann T. Genomewide screening for fusogenic human endogenous retrovirus envelopes identifies syncytin 2, a gene conserved on primate evolution. Proc Natl Acad Sci U S A. 2003 Oct 28;100(22):13013-8. doi: 10.1073/pnas.2132646100. Epub 2003 Oct 13. PMID: 14557543; PMCID: PMC240736. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC240736/pdf/10013013.pdf
6- Mangeney M, Renard M, Schlecht-Louf G, Bouallaga I, Heidmann O, Letzelter C, Richaud A, Ducos B, Heidmann T. Placental syncytins: genetic disjunction between the fusogenic and immunosuppressive activity of retroviral envelope proteins. Proc Natl Acad Sci U S A 2007; 104:20534–20539. PMID: 18077339 PMCID: PMC2154466 DOI: 10.1073/pnas.0707873105. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2154466/pdf/zpq20534.pdf
7- Harris JR. Placental endogenous retrovirus (ERV): structural, functional, and evolutionary significance. Bioessays. 1998; 20: 307-316 PMID: 9619102 DOI: 10.1002/(SICI)1521-1878(199804)20:4<307::AID-BIES7>3.0.CO;2-M https://pubmed.ncbi.nlm.nih.gov/9619102/
8- Gong R, Peng X, Kang S, Feng H, Huang J, Zhang W, Lin D, Tien P, Xiao G. Structural characterization of the fusion core in syncytin, envelope protein of human endogenous retrovirus family W. Biochem Biophys Res Commun. 2005 Jun 17;331(4):1193-200. doi: 10.1016/j.bbrc.2005.04.032. PMID: 15883002; PMCID: PMC7092852. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7092852/pdf/main.pdf
9- Cheynet V, Ruggieri A, Oriol G, Blond JL, Boson B, Vachot L, Verrier B, Cosset FL, Mallet F. Synthesis, assembly, and processing of the Env ERVWE1/syncytin human endogenous retroviral envelope. J Virol. 2005 May;79(9):5585-93. doi: 10.1128/JVI.79.9.5585-5593.2005. PMID: 15827173; PMCID: PMC1082723. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1082723/pdf/1588-04.pdf
10- Walls AC, Park YJ, Tortorici MA, Wall A, McGuire AT and Veesler D. Structure, Function, and Antigenicity of the SARS-CoV-2 Spike Glycoprotein. Cell Volume 181, Issue 2, 16 April 2020, Pages 281-292. https://doi.org/10.1016/j.cell.2020.02.058
11- Gallaher B. Response to nCoV2019 Against Backdrop of Endogenous Retroviruses. https://virological.org/t/response-to-ncov2019-against-backdrop-of-endogenous-retroviruses/396
12- Mi S Xinhua L Xiang-Ping L Geertrudia MV Finnerty H Racie L et al. Syncytin is a captive retroviral envelope protein involved in human placental morphogenesis. Nature. 2000; 403: 785-789 PMID: 10693809 DOI: 10.1038/35001608 https://www.nature.com/articles/35001608
13- Chie-Pein Chen, Liang-Fu Chen, Su-Ray Yang, Chia-Yu Chen, Chun-Chuan Ko, Geen-Dong Chang, Hungwen Chen, Functional Characterization of the Human Placental Fusogenic Membrane Protein Syncytin 2, Biology of Reproduction, Volume 79, Issue 5, 1 November 2008, Pages 815–823, https://doi.org/10.1095/biolreprod.108.069765
14- Grandi N, Tramontano E. HERV Envelope Proteins: Physiological Role and Pathogenic Potential in Cancer and Autoimmunity. Front Microbiol. 2018 Mar 14;9:462. doi: 10.3389/fmicb.2018.00462. PMID: 29593697; PMCID: PMC5861771. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5861771/pdf/fmicb-09-00462.pdf
15- Tseng CT, Sbrana E, Iwata-Yoshikawa N, Newman PC, Garron T, Atmar RL, Peters CJ, Couch RB. Immunization with SARS coronavirus vaccines leads to pulmonary immunopathology on challenge with the SARS virus. PLoS One. 2012;7(4):e35421. doi: 10.1371/journal.pone.0035421. PMID: 22536382; PMCID: PMC3335060. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3335060/pdf/pone.0035421.pdf
16- Bolles M, Deming D, Long K, Agnihothram S, Whitmore A, Ferris M, Funkhouser W, Gralinski L, Totura A, Heise M, Baric RS. A double-inactivated severe acute respiratory syndrome coronavirus vaccine provides incomplete protection in mice and induces increased eosinophilic proinflammatory pulmonary response upon challenge. J Virol. 2011 Dec;85(23):12201-15. doi: 10.1128/JVI.06048-11. PMID: 21937658; PMCID: PMC3209347. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3209347/pdf/zjv12201.pdf
17- Keith JC Jr, Pijnenborg R, Van Assche FA. Placental syncytin expression in normal and preeclamptic pregnancies. Am J Obstet Gynecol. 2002 Oct;187(4):1122-3; author reply 1123-4. doi: 10.1067/mob.2002.128512. PMID: 12389018. https://www.ajog.org/article/S0002-9378(02)70072-0/fulltext
18- Knerr I, Beinder E, Rascher W. Syncytin, a novel human endogenous retroviral gene in human placenta: evidence for its dysregulation in preeclampsia and HELLP syndrome. Am J Obstet Gynecol 2002; 186:210–213. PMID: 11854637 DOI: 10.1067/mob.2002.119636 https://www.ajog.org/article/S0002-9378(02)11228-2/fulltext
19- Lee X, Keith JC Jr, Stumm N, Moutsatsos I, McCoy JM, Crum CP, Genest D, Chin D, Ehrenfels C, Pijnenborg R, van Assche FA, Mi S. Downregulation of placental syncytin expression and abnormal protein localization in pre-eclampsia. Placenta 2001; 22:808-812. PMID: 11718567 DOI: 10.1053/plac.2001.0722 https://linkinghub.elsevier.com/retrieve/pii/S0143-4004(01)90722-2
20- Chen CP, Wang KG, Chen CY, Yu C, Chuang HC, Chen H. Altered placental syncytin and its receptor ASCT2 expression in placental development and pre-eclampsia. BJOG 2006; 113:152–158. PMID: 16411991 DOI: 10.1111/j.1471-0528.2005.00843.x. https://obgyn.onlinelibrary.wiley.com/doi/full/10.1111/j.1471-0528.2005.00843.x
21- Bjerregaard, B., Lemmen, J.G., Petersen, M.R. et al. Syncytin-1 and its receptor is present in human gametes. J Assist Reprod Genet 31, 533–539 (2014). https://doi.org/10.1007/s10815-014-0224-1
22- Cavagnari BM. Regulación de la expresión génica: cómo operan los mecanismos epigenéticos. Regulation of gene expression: how do epigenetic mechanisms work. Arch Argent Pediatr 2012;110(2):132-136. Departamento de Pediatría. Hospital Alemán.Ciudad Autónoma de Buenos Aires :https://www.sap.org.ar/docs/publicaciones/archivosarg/2012/v110n2a08.pdf
23- The Nobel Prize in Physiology or Medicine 2006. NobelPrize.org. https://www.nobelprize.org/prizes/medicine/2006/7474-the-nobel-prize-in-physiology-or-medicine-2006-2006-4/
24- Dunlap KA, Palmarini M, Varela M, Burghardt RC, Hayashi K, Farmer JL, and Spencer TE. Endogenous retroviruses regulate periimplantation placental growth and differentiation PNAS September 26, 2006 103 (39) 14390-14395; https://doi.org/10.1073/pnas.0603836103 https://www.pnas.org/content/pnas/103/39/14390.full.pdf
25- Voisset C, Blancher A, Perron H, Mandrand B, Mallet F, Paranhos-Baccala G. Phylogeny of a novel family of human endogenous retrovirus sequences, HERV-W, in humans and other primates. AIDS Res Hum Retroviruses. 1999; 15: 1529-1533(15-19) PMID: 10580403 DOI: 10.1089/088922299309810 https://pubmed.ncbi.nlm.nih.gov/10580403/
26- Henke C, Ruebner M, Faschingbauer F, et al. Regulation of murine placentogenesis by the retroviral genes Syncytin-A, Syncytin-B and Peg10. Differentiation; Research in Biological Diversity. 2013 Apr-Jun;85(4-5):150-160. DOI: 10.1016/j.diff.2013.02.002. https://europepmc.org/article/med/23807393
27- Short-term and long-term modulation of gene expression by antisense therapeutics Peter Sazani, Marla M Vacek and Ryszard Kole. Current Opinion in Biotechnology Volume 13, Issue 5, 1 October 2002, Pages 468-472.https://doi.org/10.1016/S0958-1669(02)00366-X https://pubmed.ncbi.nlm.nih.gov/12459339/
28- Cardozo T and Veazey R . Informed consent disclosure to vaccine trial subjects of risk of COVID‐19 vaccines worsening clinical disease. International Journal of Clinical Practice, October 28, 2020 DOI: 10.111/ijcp.13795 https://doi.org/10.1111/ijcp.13795 https://onlinelibrary.wiley.com/doi/10.1111/ijcp.13795
29- Susanne Rauch, Nicole Roth, Kim Schwendt, et al. mRNA based SARS-CoV-2 vaccine candidate CVnCoV induces high levels of virus neutralizing antibodies and mediates protection in rodents. doi: https://doi.org/10.1101/2020.10.23.351775 https://www.biorxiv.org/content/10.1101/2020.10.23.351775v1.full.pdf
30- Summerton J. Morpholino antisense oligomers: the case for an RNase H-independent structural type. Biochim Biophys Acta. 1999 Dec 10;1489(1):141-58. doi: 10.1016/s0167-4781(99)00150-5. PMID: 10807004.https://pubmed.ncbi.nlm.nih.gov/10807004/
31- Dolei A. The aliens inside us: HERV-W endogenous retroviruses and multiple sclerosis. Mult Scler. 2018 Jan;24(1):42-47. doi: 10.1177/1352458517737370. PMID: 29307292. https://pubmed.ncbi.nlm.nih.gov/29307292/
32- Antony JM, Deslauriers AM, Bhat RK, Ellestad KK, Power C. Human endogenous retroviruses and multiple sclerosis: innocent bystanders or disease determinants? Biochim Biophys Acta. 2011 Feb;1812(2):162-76. doi: 10.1016/j.bbadis.2010.07.016. Epub 2010 Aug 6. PMID: 20696240; PMCID: PMC7172332. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7172332/pdf/main.pdf
33- Arru G, Mameli G, Deiana GA, Rassu AL, Piredda R, Sechi E, Caggiu E, Bo M, Nako E, Urso D, Mariotto S, Ferrari S, Zanusso G, Monaco S, Sechi G, Sechi LA. Humoral immunity response to human endogenous retroviruses K/W differentiates between amyotrophic lateral sclerosis and other neurological diseases. Eur J Neurol. 2018 Aug;25(8):1076-e84. doi: 10.1111/ene.13648. Epub 2018 May 14. PMID: 29603839. https://pubmed.ncbi.nlm.nih.gov/29603839/
34- Alfahad T, Nath A. Retroviruses and amyotrophic lateral sclerosis. Antiviral Res. 2013 Aug;99(2):180-7. doi: 10.1016/j.antiviral.2013.05.006. Epub 2013 May 23. PMID: 23707220; PMCID: PMC3723705. https://pubmed.ncbi.nlm.nih.gov/23707220/
35- Küry P, Nath A, Créange A, Dolei A, Marche P, Gold J, Giovannoni G, Hartung HP, Perron H. Human Endogenous Retroviruses in Neurological Diseases. Trends Mol Med. 2018 Apr;24(4):379-394. doi: 10.1016/j.molmed.2018.02.007. Epub 2018 Mar 15. PMID: 29551251; PMCID: PMC7185488. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7185488/pdf/main.pdf
36- Levet S, Charvet B, Bertin A, Deschaumes A, Perron H, Hober D. Human Endogenous Retroviruses and Type 1 Diabetes. Curr Diab Rep. 2019 Nov 21;19(12):141. doi: 10.1007/s11892-019-1256-9. PMID: 31754894; PMCID: PMC6872510. https://pubmed.ncbi.nlm.nih.gov/31754894/
L’informazione libera e indipendente ha bisogno del tuo aiuto. Ora più che mai… Database Italia non riceve finanziamenti e si mantiene sulle sue gambe. La continua censura, blocchi delle pubblicità ad intermittenza uniti agli ultimi attacchi informatici non ci permettono di essere completamente autosufficienti.
Fai una donazione seguendo il link sicuro qui sotto
SOSTIENI DATABASE ITALIA